Un certain nombre de substances comme la carnitine, la glutamine, la choline, l’inositol et l’acide lipoïque, bien que leur synthèse endogène soit possible, doivent être apportées par l’alimentation et peuvent être rapprochées des vitamines.
L-Carnitine
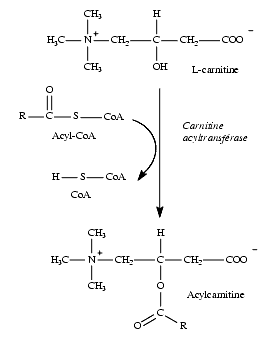
La L-carnitine ou triméthylaminohydroxybutyrate est nécessaire à la pénétration des acides gras à chaîne longue dans les mitochondries où ils sont métabolisés par b-oxydation. C’est la fonction alcool de la carnitine qui intervient dans l’estérification des acides gras.
Métabolisme
Origine
La L-carnitine présente dans l’organisme a deux origines : l’une exogène par apport alimentaire et l’autre endogène par biosynthèse.
La carnitine est présente dans les aliments, notamment les viandes et les laitages. Son absorption digestive, lors d’un apport normal, se fait par un mécanisme actif. Lorsqu’il existe des concentrations élevées dans le tube digestif, une absorption passive apparaît. Lorsque la synthèse endogène est ralentie, l’absorption digestive augmente. On considère qu’un apport de 10 mg/jour chez l’adulte serait nécessaire pour assurer les besoins.
La biosynthèse de carnitine s’effectue dans le foie, le rein, le cerveau, à partir de la lysine qui subit d’abord une triméthylation sous l’influence d’une lysine-méthylase en présence de 5-adénosyl-méthionine. La triméthyl-lysine subit plusieurs biotransformations avant de donner la carnitine. La biosynthèse de carnitine nécessite la présence de S-adénosyl-méthionine, d’acide ascorbique, de NAD et FAD, de pyridoxine et de fer ferreux.
Distribution
La concentration plasmatique de L-carnitine libre est comprise entre 30 à 70 totale (libre et estérifiée) entre 40 à 80
Les tissus riches en carnitine sont les muscles cardiaques et squelettiques, le tissu adipeux et surtout l’épididyme et le liquide séminal. La concentration de carnitine s’élève dans l’épididyme sous l’influence de la testostérone. Ces derniers tissus ne synthétisent pas la carnitine, mais la captent à partir du plasma. Il y a compétition pour cette captation entre la carnitine elle-même et des analogues structuraux portant une fonction triméthylamine.
Élimination
La carnitine s’élimine dans les urines où on trouve de 100 à 250 24 h sous forme totale. L’élimination de carnitine est plus élevée chez l’homme que chez la femme.
La carnitine libre est normalement réabsorbée au niveau du tubule rénal, ce qui en limite les pertes. Chez les malades hémodialysés, les pertes sont importantes et il peut être nécessaire de leur apporter une supplémentation.
La carnitine s’élimine aussi sous forme d’acylcarnitine (l’acyl pouvant être un acide gras endogène ou un médicament comme l’acide valproïque ou l’acide pivaloyl présent dans la pivampicilline).
Effets
La carnitine assure la translocation des acides gras à chaîne longue dans la mitochondrie alors que les acides gras à chaîne courte ou moyenne y pénètrent directement.
Les acides gras, R-COOH, à chaîne longue présents dans le cytosol, en présence d’ATP et de CoA-SH, sont transformés en acyl-CoA que l’on peut écrire R-CO-S-CoA.
La carnitine acyltransférase I, présente au niveau de la partie externe de la membrane de la mitochondrie, assure la fixation du groupe acyl sur la carnitine qui devient ainsi l’acyl-carnitine, R-CO-carnitine.
L’enzyme carnitine-acylcarnitine translocase transmembranaire permet la pénétration de l’acyl carnitine, R-CO-carnitine, à l’intérieur de la mitochondrie ainsi que la sortie de la carnitine de la mitochondrie. En cas de déficience en translocase, les « acyl-carnitine » ne pénètrent pas dans les mitochondries, leur concentration s’élève dans les tissus et leur élimination urinaire augmente.
La carnitine acyl-transférase II liée à la partie interne de la membrane mitochondriale hydrolyse l’acyl-carnitine en acyl, R-COOH, qui est estérifié par le CoA-SH pour donner un acyl-CoA, R-CO-S-CoA, et en carnitine qui retourne dans le compartiment cytosolique.
Dans la mitochondrie, les acyl-CoA, R-CO-S-CoA, libèrent par ß-oxydations successives des acétyl-CoA qui entrent dans le cycle de Krebs, fournissant de l’énergie à la cellule. Ils sont aussi à l’origine des corps cétoniques.
En réalité, plusieurs types de carnitine acyltransférase ont été décrites en fonction de leur spécificité pour l’acyl : à longue chaîne (palmitoyl C 16), à chaîne moyenne (octanoyl C 8), à chaîne branchée dérivant de la valine, la leucine et l’isoleucine, et à chaîne courte.
Carence
La déficience en carnitine, rarement d’origine alimentaire, est le plus souvent d’origine endogène par trouble de son métabolisme : biosynthèse défectueuse, élimination rénale excessive ou consommation augmentée du fait de la présence d’une grande quantité d’acides organiques.
Elle peut se traduire par des troubles musculaires et cardiaques :
- musculaires : faiblesse, myalgies lors des efforts; il peut y avoir infiltration graisseuse des muscles
- cardiaques : cardiomyopathie.
Sur le plan biologique, il y a une diminution considérable de la concentration de carnitine dans les tissus mais la concentration plasmatique n’est pas toujours abaissée.
Les symptômes du syndrome de Reye ressemblent à ceux d’une déficience en carnitine bien que la concentration plasmatique en carnitine soit normale de même que sa concentration tissulaire.
Utilisation
La prise de L-carnitine par les sujets normaux, même à très fortes doses, n’a entraîné ni effets indésirables ni effets bénéfiques.
Les préparations pharmaceutiques à base de DL-carnitine, forme racémique, peuvent entraîner un syndrome de type myasthénique car la D-carnitine non active entre en compétition avec la L-carnitine active. La DL-carnitine ne doit plus être utilisée.
La L-carnitine est indiquée dans le traitement des déficiences avérées, par exemple celle de certains hémodialysés.
Son utilisation dans diverses maladies chroniques ou d’évolution défavorable n’a pas donné de résultats très encourageants.
La L-carnitine semble potentialiser les effets des glucocorticoïdes et de la thyroxine sur la synthèse de dipalmoyl-phosphatidyl-choline, principal composant du surfactant dont la déficience joue un rôle dans le syndrome de détresse respiratoire du nouveau-né.
Comme il y a normalement beaucoup de carnitine dans le liquide séminal, son utilisation dans certaines stérilités masculines a été proposée.
Enfin, la carnitine est utilisée pour tenter d’améliorer les performances sportives des hommes et des chevaux, mais on ne dispose pas d’étude convaincante quant à son efficacité.
L-glutamine
La L-glutamine est un acide aminé synthétisé par l’organisme et apporté par l’alimentation. Elle est présente à l’intérieur des cellules et dans le milieu extracellulaire
La glutamine est indispensable aux étapes initiales de la synthèse des nucléotides puriques et pyrimidiques. Elle peut être transformée en glutamate et participe à des réactions de transamination. Elle intervient dans la synthèse d’inosine monophosphate par l’intermédiaire de la glutamine-phosphoryl-pyrophosphate amidotransférase.
Chez les malades nécessitant une alimentation parentérale apportant des acides aminés sans glutamine on a observé une chute importante des réserves tissulaires en glutamine ainsi qu’une altération de la paroi de l’intestin grêle.
L’administration de glutamine par voie parentérale, en complément de l’apport des acides aminés habituels, améliore l’état des malades, diminue les infections et la mortalité.
La glutamine elle-même étant peu soluble et instable en solution, des préparations susceptibles de libérer de la glutamine dans l’organisme ont été préparées. Il s’agit de dipeptides, la L-glycine-L-glutamine et la L-alanyl-L- glutamine qui, après administration par voie intraveineuse sont hydrolysés dans le plasma, libérant ainsi la glutamine. En france le dipeptide disponible est la L-alanyl-L-glutamine.
L’apport de L-glutamine est indiqué comme complément à la nutrition parentérale habituelle pour compenser la déficience en glutamine qui survient chez certains malades en réanimation.
Inositol
L’inositol est un isomère du glucose. Parmi les isomères, le myo-inositol est le produit biologiquement actif.
L’apport alimentaire quotidien d’inositol est de 1 g/jour environ. Il est bien absorbé par le tube digestif. Le lait humain est très riche en inositol. L’organisme a également la possibilité de synthétiser l’inositol à partir du glucose et inversement de transformer l’inositol en glucose.
La concentration plasmatique normale d’inositol est d’environ 5 mg/L mais sa concentration dans le coeur, le muscle squelettique et le cerveau est très élevée.
Dans l’organisme, l’inositol existe sous forme libre et sous forme de dérivés phosphorylés en particulier les phospho-inositides.
Il y a peu d’inositol dans l’urine sauf chez les diabétiques.
L’inositol comme la choline est présent dans les phospholipides membranaires. Les phospho-inositides dont le 1-4-5 inositol triphosphate ou IP3 jouent un rôle essentiel dans les communications intracellulaires en modulant la concentration de calcium (Voir « Rôle de la phospholipase C ».).
L’inositol intervient dans la mobilisation lipidique et dans la synthèse de surfactant.
La déficience en inositol, chez les rongeurs, provoque une chute des poils, une dermatose exsudative et une accumulation graisseuse au niveau hépatique et intestinal.
La prescription d’inositol aurait un effet bénéfique chez les prématurés en nutrition parentérale en état de détresse respiratoire.
Acide lipoïque
L’acide lipoïque ou acide thioctique comporte deux atomes de soufre. Il existe sous une forme oxydée qui est un disulfure cyclique et sous une forme réduite appelée acide dihydrolipoïque, non cyclique.
L’acide lipoïque est présent dans les tissus végétaux et animaux. Chez l’homme il est d’origine exogène, alimentaire, et probablement endogène mais les réactions impliquées dans sa biosynthèse sont mal connues. L’acide lipoïque est métabolisé principalement par ß-oxydation.
L’acide lipoïque est le coenzyme des déshydrogénases : la pyruvate déshydrogénase qui assure la transformation du pyruvate en acétyl-CoA et de l’a-cétoglutarate déshydrogénase qui assure la transformation de l’a-cétoglutarate en succinyl-CoA. Dans ces réactions, d’autres coenzymes, le NAD, le FAD, la thiamine pyrophosphate, interviennent également.
L’acide lipoïque intervient de plus dans la néoglycogenèse, dans le métabolisme de la glycine et dans celui de certaines prostaglandines.
L’acide lipoïque n’est pas commercialisé en tant que médicament.
Choline
La choline ou triméthyléthanolamine comporte une fonction ammonium quaternaire (CH3)3–N+–CH2–CH2OH. Elle est présente dans les végétaux, les graisses animales et le jaune d’uf, essentiellement sous forme estérifiée comme dans la lécithine (phosphatidylcholine).
La choline libre, non estérifiée, est incomplètement absorbée par le tube digestif. Elle est mieux absorbée sous forme de glycérophosphocholine.
Une biosynthèse endogène de la choline par trans-méthylation de l’éthanolamine est possible.
La choline est un constituant des phospholipides et, par conséquent, des membranes biologiques. Elle est présente en quantité importante dans le cerveau.
La choline ainsi que la bétaïne qui sont des donneurs de groupe méthyl favorisent la transformation de l’homo-cystéine en méthionine.
La choline est nécessaire à la synthèse d’acétylcholine. Sa pénétration dans le cerveau s’effectue par diffusion facilitée et est dépendante de sa concentration plasmatique. Quand celle-ci augmente, sa concentration et celle d’acétylcholine augmentent dans le cerveau. Cette constatation a été à l’origine de divers essais de traitement de la maladie d’Alzeimer où une déficience en acétylcholine existe. La choline intervient aussi dans la synthèse du PAF.
La déficience en choline apparaît surtout comme une déficience en groupe méthyl.
Chez le rat, une déficience en choline pendant la gestation provoque dans la descendance des troubles de l’apprentissage pendant toute la vie.
La choline diminue l’accumulation de lipides dans le foie des animaux diabétiques. L’inositol, la méthionine, la vitamine B12, l’acide folique agissent comme la choline et renforcent son action.
Le rôle hépatoprotecteur de la choline a été mis en évidence sur des animaux rendus diabétiques par pancréatectomie.
La citicoline, ester de la cytidine pyrophosphate et de la choline, agirait comme donneur de choline et protégerait la membrane cellulaire.
Elle est proposée dans le traitement des traumatismes craniens.
Créatine
La créatine est une molécule synthétisée par l’organisme à partir de l’arginine et de la glycine et apportée par l’alimentation, notamment la viande et le poisson. On considère que l’organisme en synthétise 1 à 2 g par jour et que l’alimentation en apporte autant. Elle pénètre dans les cellules musculaires grâce à un transporteur spécifique sodium dépendant
Dans l’organisme, la créatine, en présence d’ATP, est transformée en phosphocréatine ou créatine phosphate, appelée aussi phosphagène ; la phosphocréatine peut transférer son groupe phosphate à l’ADP pour le transformer en ATP, selon la réaction :
![]()
La phosphocréatine permet la régénération d’ATP, lorsque ce dernier est consommé comme source d’énergie pour la contraction musculaire.
La créatine et la phosphocréatine sont métabolisées par cyclisation en créatinine.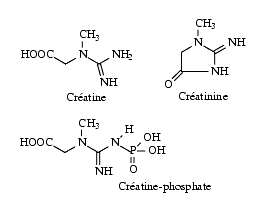
La phosphocréatine a été commercialisée comme médicament proposé dans le traitement adjuvant de l’insuffisance cardiaque.
La créatine n’est pas commercialisée comme médicament. Elle est utilisée par voie buccale, à dose élevée, de l’ordre de 20 g par jour, par certains athlètes en vue d’améliorer leurs performances physiques.
On ne dispose pas pour le moment de données suffisantes pour évaluer l’effet de la créatine sur les performances physiques et sa tolérance en utilisation répétée ou prolongée à forte dose.
- Précédent
- Suivant