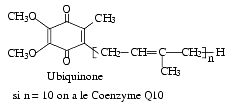La vitamine B2 ou riboflavine a été découverte en 1932. Elle joue un rôle extrêmement important dans les transferts d’électrons après transformation en flavine mononucléotide, FMN, et flavine-adénine dinucléotide, FAD.
Structure
La riboflavine est un dérivé de l’isoalloxazine, substitué en C5 par un sucre, le ribitol (ribose + flavine = riboflavine), qui est phosphorylé pour donner la flavine mononucléotide, ou FMN, et la flavine-adénine dinucléotide, ou FAD.
La riboflavine est sensible à la lumière qui la décompose. Elle forme des complexes avec les métaux comme l’argent, le cuivre et le mercure.
La propriété essentielle du noyau isoalloxazine est de participer à des transferts d’électrons, soit d’un électron, soit de deux électrons à la fois. Elle participe à l’oxydoréduction de l’oxygène moléculaire en H2O2 et à son clivage.
Sous forme oxydée le noyau est plan et sous forme réduite il se plie en forme de toit.
Les flavines réduites sont des donneurs d’électrons au fer des cytochromes, à l’oxygène moléculaire qui devient, par acceptation d’un électron, le radical superoxyde O2·-, de deux électrons, le peroxyde O22- (H2O2) et de quatre électrons, l’ion O2-.
Métabolisme
L’absorption de la riboflavine s’effectue dans la partie haute du tractus gastro-intestinal. Elle est proportionnelle à la dose ingérée jusqu’à environ 25 mg/jour et est sodium-dépendante.
Les besoins journaliers sont de 1 à 2 mg/jour. On trouve de la riboflavine dans de nombreux aliments, laitages, viandes, poissons, champignons. La riboflavine est stable à la chaleur et n’est pas détruite par la cuisson mais est décomposée à la lumière, probablement par des réactions faisant intervenir le radical OH.
La concentration de riboflavine totale (vitamine B2 + FMN + FAD) est de 50 à 100 25 à 40 taire étant de 180 à 260
La concentration dans les tissus est beaucoup plus élevée, il y a 25 mg/kg dans le foie et environ 10 mg/kg dans le coeur.
La concentration de riboflavine dans le cerveau est maintenue constante, même lorsque les apports sont très faibles, et n’augmente pas lorsque les apports sont très élevés.
Dans la cellule intestinale et le foie, la riboflavine, sous l’influence d’une flavokinase et en présence d’ATP, est transformée en flavine mononucléotide ou FMN, elle-même transformée ensuite en flavine-adénine dinucléotide ou FAD. Les réactions inverses, sous l’influence des riboflavine phosphatases, sont possibles La riboflavine est active après transformation en FMN et en FAD.
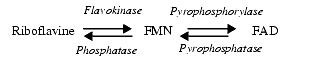
L’activité de la flavokinase est stimulée par les hormones thyroïdiennes et l’aldostérone, et inhibée par certains médicaments comme les neuroleptiques phénothiaziniques, notamment la chlorpromazine dont la structure ressemble à celle de la riboflavine.
La riboflavine et ses métabolites s’éliminent essentiellement dans l’urine qu’elles colorent en jaune. Lorsque l’élimination urinaire est inférieure à 50 en vitamine B2 est probable
Effets
La riboflavine participe au transfert d’électrons par l’intermédiaire du FMN et du FAD qui sont en contact étroit avec les enzymes. Contrairement au NAD qui assure le transfert simultané de deux électrons, les flavines assurent le transfert soit d’un soit de deux électrons.
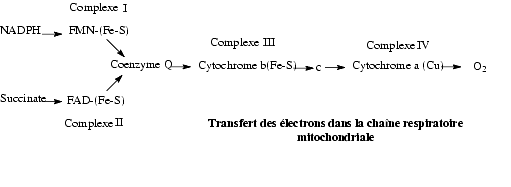
- Dans la chaîne respiratoire mitochondriale
- Le FMN et le FAD, sous forme de flavoprotéines, assurent l’entrée des électrons (hydrogène) dans la chaîne respiratoire. Le FMN reçoit les électrons du NADH, le FAD reçoit les électrons du succinate par la succinate deshydrogénase, et de l’acétyl-CoA par l’intermédiaire de l’acétyl-CoA déshydrogénase. Ces deux flavoprotéines transfèrent les électrons à l’ubiquinone ou coenzyme Q qui, elle-même, les transfère à son tour aux cytochromes
- Dans diverses biotransformations comportant une oxydoréduction, le FMN et le FAD jouent le rôle de donneur ou d’accepteur d’électrons (hydrogène).
Les flavoprotéines interviennent au niveau de différentes enzymes, monoamine oxydase, xanthine oxydase, aldéhyde oxydase, glutathion réductase et de nombreuses déshydrogénases.
Carence
Les signes de carence sont frustes, on observe surtout des atteintes cutanéo-muqueuses :
- lèvres brillantes, sèches, rouges avec croûtes et fissures.
- stomatite avec langue pourpre et atrophie des papilles.
- larmoiement, hypervascularisation conjonctivale, photophobie, cataracte.
- séborrhée au niveau de la face.
Une anémie normochrome peut également se voir.
La carence en vitamine B2 pendant la grossesse augmente le risque de malformations chez l’enfant.
La carence en vitamine B2 est mesurée par l’activité de la
glutathion réductase érythrocytaire, en absence et après addition de FAD. Si l’activation en présence de FAD est supérieure à 20%, on considère qu’il y a carence.
Utilisation
Une carence isolée en riboflavine est rare et, en pratique, on prescrit peu la riboflavine seule mais souvent une association de vitamine B.
- Le cytochrome Q ou ubiquinone, participe au transfert des électrons dans la chaîne respiratoire mitochondriale (voir schéma). Il est constitué d’un noyau quinone, dont la biosynthèse s’effectue à partir de la tyrosine, et d’une chaîne latérale formée le plus souvent de 10 unités isopréniques, dont la biosynthèse s’effectue à partir du farnesyl pyrophosphate qui constitue un maillon dans la synthèse du cholestérol.
- Lorsqu’il comporte 10 unités d’isoprène, on le désigne par le terme coenzyme Q 10 (Co Q 10), appelé également ubidécarénone.
- Présent dans la mitochondrie, le Co Q 10 est un maillon du transfert d’électrons en passant par la forme ubiquinol, ubiquinone et ubisemiquinone. Le Co Q 10 est aussi présent au niveau de la membrane plasmique et de divers organites intracellulaires. Il peut avoir un effet anti-oxydant ou pro-oxydant.
- Lorsqu’il comporte 10 unités d’isoprène, on le désigne par le terme coenzyme Q 10 (Co Q 10), appelé également ubidécarénone.
- Le Co Q 10 a donné des résultats intéressants dans le traitement de certaines cardiomyopathies et dans la prévention de la cardiotoxicité des antinéoplasiques de type anthracyclines.
- L’idébénone est un dérivé de l’ubiquinone proposé dans le traitement des accidents vasculaires cérébraux.
- L’ubidécarénone et l’idébénone sont commercialisés dans certains pays dont l’Italie sous les noms respectifs de IUVACOR* et MNESIS*.
- L’atovaquone est une molécule ayant une analogie structurale avec l’ubiquinone. Elle inhibe le transfert des électrons au niveau du complexe III de certains parasites comme Pneumocystis carinii, Plasmodium falciparum et Toxoplasma gondii. Elle peut être utilisée dans le traitement des infections correspondantes. La biodisponibilité de l’atovaquone est faible mais elle est multipliée par environ trois lorsqu’elle est prise en même temps qu’un repas riche en lipides.
- Ses principaux effets indésirables sont des éruptions, des troubles digestifs, des céphalées…
- Ses principaux effets indésirables sont des éruptions, des troubles digestifs, des céphalées…