Biosynthèse
L’insuline est produite dans les cellules ß qui constituent 75% des îlots de Langerhans du pancréas. Les cellules a sécrètent le glucagon, les cellules d la somatostatine.
L’insuline est synthétisée sous forme d’une chaîne polypeptidique unique : la préproinsuline qui se transforme en proinsuline qui, elle-même, sous l’influence de protéases appelées furines, donne l’insuline et le peptide C (C pour connecting, car reliant les deux chaînes A et B). Liée à deux atomes de zinc, elle est stockée dans des granules sous forme d’un polymère, probablement un hexamère.
Sécrétion
L’insuline, ainsi que le peptide C, est libérée par exocytose dans la veine pancréatico-duodénale qui la conduit directement au foie, lequel en conserve ou détruit près de 50%. Le reste de l’insuline se distribue dans l’ensemble de l’organisme.
Sur un fond de sécrétion continue d’environ 40 jeun, il y a des augmentations de sécrétion liées aux repas. A ces variations se superposent des pointes de sécrétion de type pulsatile. Le but du traitement substitutif par l’insuline exogène est de se rapprocher de la courbe de sécrétion physiologique.
Le principal stimulant de la sécrétion d’insuline est le glucose; il provoque une libération biphasique : un effet immédiat de courte durée et un effet prolongé. Les canaux jonctionnels, en permettant le passage d’ions, de métabolites, de messagers secondaires d’une cellule à l’autre, jouent un rôle important pour synchroniser sa sécrétion.
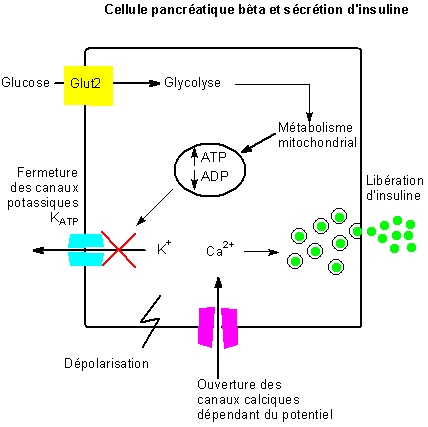
La stimulation de la sécrétion d’insulinepar le glucose nécessite plusieurs étapes :
- sa pénétration dans la cellule ß, pénétration par les transporteurs Glut2,indépendante de la présence d’insuline.
- sa phosphorylation par une glucokinase présente dans les cellules ß puis sa métabolisation avec synthèse d’ATP dont la concentration intracellulaire augmente. Cette augmentation d’ATP entraîne la fermeture des canaux potassiques ATP-dépendants et donc l’arrêt de la sortie de potassium, ce qui entraîne une dépolarisation à l’origine de l’ouverture des canaux calcium voltage-dépendants. L’entrée du calcium provoque l’activation de phospholipases A2 et C et la sécrétion d’insuline.
Les autres stimulants de la sécrétion d’insuline sont les acides aminés (arginine, lysine), les acides gras et les corps cétoniques.
Des hormones, autres que l’insuline, et des médiateurs modulent la sécrétion d’insuline.
- les catécholamines par effet ß2-mimétique. Les ß-bloqueurs pourraient théoriquement aggraver l’hyperglycémie en diminuant la sécrétion d’insuline mais, en réalité, ils inhibent surtout l’effet hyperglycémiant des catécholamines et aggravent l’hypoglycémie.
- l’acétylcholine et diverses hormones d’origine intestinale : gastrine, sécrétine, cholécystokinine, glucagon.
D’autres la diminuent :
- les sympathomimétiques à effet a2, dont les antihypertenseurs à effet central qui peuvent ainsi aggraver l’hyperglycémie.
- la somatostatine qui inhibe la sécrétion d’insuline et de glucagon et pourrait participer à la régulation de leur sécrétion. Elle est présente dans les cellules d du pancréas. A doses élevées, la somatostatine inhibe aussi la libération de plusieurs autres hormones dont l’hormone de croissance et la TSH. Elle inhibe également l’absorption et la motilité intestinales. La sécrétion de somatostatine est stimulée par le glucose, divers acides aminés et diverses hormones intestinales.
- la leptine ou OB protéine, en agissant sur des récepteurs OB du pancréas.
Distribution
Après injection intraveineuse, la demi-vie de l’insuline dans le plasma est d’environ six minutes chez le sujet normal et chez le diabétique. Son volume de distribution est égal au volume du liquide extracellulaire, soit environ 20% du poids corporel. C’est essentiellement la forme monomère de l’insuline qui diffuse dans les tissus. L’insuline peut traverser la barrière hémato-encéphalique grâce à des transporteurs.
Catabolisme
L’insuline est inactivée par des biotransformations enzymatiques : hydrolyse par des métalloprotéinases et réduction, c’est-à-dire rupture des liaisons S – S. L’élimination rénale d’insuline est faible car, après filtration, elle est réabsorbée par le tubule.
