Les folates sous forme réduite, acide tétrahydrofolique, sont impliqués dans les réactions enzymatiques de transfert des groupes monocarbonés, ce qui nécessite que leur réduction par la dihydrofolate réductase soit assurée. L’acide tétrahydrofolique, après avoir fixé un groupe monocarboné, le cède à un substrat au cours d’une réaction enzymatique.
Il intervient ainsi dans la synthèse de l’ADN en permettant la synthèse de déoxythymidine et des bases puriques ainsi que dans d’autres réactions.
Synthèse d’une base pyrimidique : la déoxythymidine
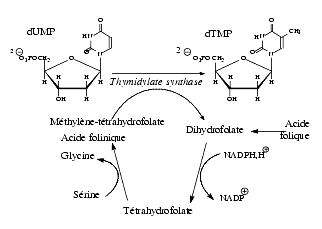
La synthèse de déoxythymidine monophosphate, dTMP ou simplement TMP, à partir du déoxyuridilate-monophosphate, dUMP, est catalysée par la thymidylate synthase. Cette réaction enzymatique nécessite la présence de N5-N10-méthylène-tétrahydrofolate qui joue le rôle de donneur de groupe monocarboné et celui de réducteur par sa transformation en 7-8-dihydrofolate. Ce dernier, grâce à la tétrahydrofolate réductase, est réduit en tétrahydrofolate, lequel est transformé en N5-N10-méthylène-tétrahydrofolate sous l’influence de la sérine hydroxy-méthyl-transférase.
L’activité de la thymidylate synthase est très importante en phase de croissance cellulaire, ceci explique l’impact de la déficience en folate, sur l’hématopoïèse notamment.
Synthèse des bases puriques
La transformation du 5-phosphoribosyl-pyrophosphate, 5-PRP, en inosine 5′-monophosphate, IMP, comporte dix étapes métaboliques. Deux d’entre elles nécessitent la présence de tétrahydrofolate. L’IMP est à l’origine de la synthèse des bases puriques, adénosine, AMP, ADP, ATP, et de GMP, GDP, GTP.
Transformation de l’homocystéine en méthionine
Sous l’influence de la 5-méthyl-tétrahydrofolate-homocystéine-méthyl-transférase, l’homocystéine est transformée en méthionine, qui est elle-même en partie ensuite métabolisée en S-adénosylméthionine, coenzyme donneur du groupe méthyl dans une centaine de réactions biologiques.
Interconversion glycine-sérine
La sérine est transformée en glycine par la sérine hydroxy-méthyl transférase en présence de pyridoxal-phosphate, d’acide lipoïque et de THF qui, en acceptant le CH2OH de la sérine, est transformé en CH2OH-THF.
Catabolisme de l’histidine
La transformation de l’histidine en acide glutamique s’effectue en plusieurs étapes. La dernière consiste en la transformation de l’acide formimino-glutamique en acide glutamique par perte du groupe formimino CH-NH2 capté par le THF.
Méthylation des amines biologiques
Dans la méthylation des amines biologiques, le CH3-THF, ou plus probablement la S-adénosyl méthionine, est le donneur de méthyl.