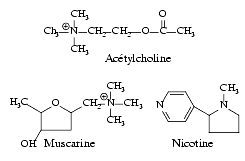
L’acétylcholine a des effets muscariniques et des effets nicotiniques par stimulation des récepteurs correspondants.
Effets muscariniques
Ils sont appelés ainsi car ils ressemblent à ceux de la muscarine, substance extraite d’un champignon.
Il existe plusieurs types de récepteurs muscariniques appelés M1, M2, M3, les plus connus, M4 et M5, couplés aux protéines G. Schématiquement, les récepteurs M1 et M3 sont couplés à la phospholipase C qui entraîne une élévation de l’inositol-triphosphate, IP3, du diacylglycérol, DAG, et du Ca2+; les récepteurs M2 sont couplés aux canaux K+ dont ils favorisent l’ouverture et à l’adénylcyclase qu’ils inhibent.
L’acétylcholine a des effets muscariniques périphériques, ce sont les mieux connus, et centraux. Ces effets sont inhibés par l’atropine.
Effets cardiaques (récepteurs M2)
L’innervation cholinergique des oreillettes est beaucoup plus importante que celle du myocarde. Une injection d’acétylcholine ou la stimulation du parasympathique provoque :
- une bradycardie allant jusqu’à l’arrêt transitoire des battements (échappement vagal) par effet sinusal.
- une diminution de la conduction auriculo-ventriculaire.
- une diminution de la force de contraction des oreillettes.
Le ralentissement cardiaque s’explique au moins en partie par l’hyperpolarisation cellulaire consécutive à l’ouverture des canaux potassiques qui sont directement liés aux protéines G et laissent sortir le potassium hors de la cellule, ce qui entraîne une augmentation de sa polarisation. La diminution de la force de contraction provient d’une diminution de l’entrée du Ca2+ dans la cellule, probablement par inhibition de l’adénylcyclase.
L’injection intraveineuse de très faibles doses d’acétylcholine chez l’animal ou chez l’homme entraîne une chute immédiate et fugace de la pression artérielle provenant du ralentissement cardiaque et de la vasodilatation.
Effets vasculaires
Les vaisseaux comportent des récepteurs muscariniques mais ne reçoivent pas d’innervation cholinergique
L’injection d’acétylcholine entraîne une vasodilatation artériolaire consécutive à la libération par l’endothélium d’une substance vasodilatatrice, appelée d’abord EDRF (endothelium derived relaxing factor) puis identifiée comme étant le monoxyde d’azote, NO.
La vasoconstriction paradoxale provoquée par l’acétylcholine sur des coronaires présentant des lésions athéromateuses s’explique par l’absence de libération d’EDRF par les cellules endothéliales lésées ou absentes et la stimulation directe de la phospholipase A2 des fibres lisses, conduisant à la libération d’acide arachidonique.
Effets sur les fibres lisses autres que vasculaires (récepteurs M3)
Par stimulation de la phospholipase C, l’acétylcholine provoque :
- au niveau de l’intestin : une augmentation du tonus avec parfois une augmentation des contractions péristaltiques. Les nausées, les vomissements témoignent de cette action stimulante.
- au niveau des uretères : une augmentation du tonus.
- au niveau des bronches : une bronchoconstriction. En aérosol, l’acétylcholine peut provoquer une crise d’asthme.
Effets sur les sécrétions (récepteurs M3)
Par action sur la phospholipase C, l’acétylcholine augmente les sécrétions digestives (salive abondante), bronchiques (encombrement bronchique), cutanées (sueurs) et lacrymales.
Effets sur l’œil (récepteurs M3)
L’acétylcholine tend à donner un myosis avec diminution du diamètre de l’iris, ce qui facilite l’écoulement de l’humeur aqueuse et tend à abaisser la pression intra-oculaire.
Effets centraux
Les effets muscariniques au niveau du système nerveux central sont complexes et encore mal connus. Selon les conditions, la stimulation des récepteurs muscariniques post-synaptiques provoque une dépolarisation ou une hyperpolarisation. Chez l’animal, leur stimulation entraîne une facilitation de l’apprentissage mais aussi une hypothermie, des tremblements, des convulsions.
Effets nicotiniques
Les effets de l’acétylcholine appelés nicotiniques ressemblent, au moins partiellement, à ceux de la nicotine et sont consécutifs à l’ouverture des récepteurs-canaux cationiques qui laissent entrer le sodium et le calcium dans la cellule, créant ainsi une dépolarisation.
Les récepteurs nicotiniques, récepteurs canaux à réponse rapide, ont une structure pentamérique. Ils sont activés par l’acétylcholine. Toutefois, ils ne sont pas strictement identiques au niveau du ganglion du système nerveux autonome, de la synapse neuromusculaire et du cerveau. On distingue ceux qui sont inhibés par la bungarotoxine A, polypeptide extrait du venin de serpent et ceux qui ne le sont pas. Mais leur fonctionnement est similaire, conduisant à une dépolarisation par entrée de sodium et de calcium dans la cellule. Les principales étapes de la transmission synaptique sont représentées dans le schéma qui suit.
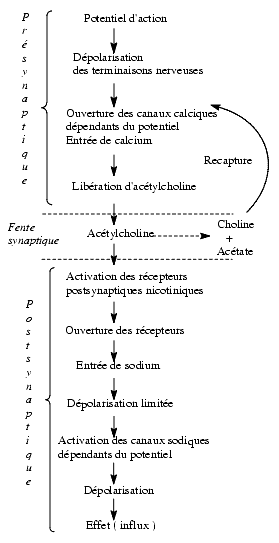
L’acétylcholine, par ses effets nicotiniques, assure la transmission synaptique. Il faut deux molécules d’acétylcholine pour activer le récepteur et ouvrir le canal.
Au niveau des ganglions du système nerveux autonome
L’acétylcholine assure la transmission interneuronale dans le système nerveux autonome. La fibre présynaptique libère de l’acétylcholine qui, par ouverture des canaux sodiques liés aux récepteurs nicotiniques, entraîne une dépolarisation à l’origine d’un nouvel influx dans la fibre postsynaptique. Cette stimulation provoque à son tour une libération d’acétylcholine par les terminaisons parasympathiques et de catécholamines par les terminaisons adrénergiques.
Au niveau neuromusculaire
La stimulation des récepteurs nicotiniques par l’acétylcholine est responsable de la transmission neuromusculaire.
Au voisinage du muscle, le nerf moteur recouvert de sa gaine de myéline se divise en un bouquet de rameaux terminaux dépourvus de myéline. Ces rameaux terminaux qui sont très riches en mitochondries et en petites vésicules synaptiques (300 à 500 Å) contenant de l’acétylcholine, serpentent dans les gouttières creusées dans le sarcoplasme et appelées gouttières synaptiques.
La stimulation d’un nerf moteur provoque la libération d’acétylcholine dans la fente synaptique de la jonction neuromusculaire. Par contre la stimulation directe du muscle, même si elle entraîne des contractions, ne provoque pas de libération d’acétylcholine.
L’acétylcholine agit sélectivement au niveau de la jonction neuromusculaire :
- apportée en faible quantité par micropipette ou électrophorèse au niveau de la plaque motrice, l’acétylcholine déclenche une contraction musculaire.
- appliquée sur le nerf ou sur le muscle (en dehors de la plaque motrice), elle n’entraîne aucun effet;
- apportée en excès au niveau de la plaque motrice, l’acétylcholine peut inhiber les contractions musculaires consécutives à la stimulation du nerf.
Le potentiel de pointe de l’axone déclenche l’apparition d’une dépolarisation localisée au niveau de la plaque motrice. Lorsque cette dépolarisation atteint un seuil suffisant, il apparaît, par ouverture des canaux cationiques voltage-dépendants, un potentiel de pointe qui se propage dans les fibres musculaires.
Les ions Ca2+ et Mg2+ interviennent : l’ion Ca2+ favorise la transmission neuromusculaire alors que l’ion Mg2+ tend à s’y opposer.
- La myasthénie (Myasthenia gravis) se traduit par une faiblesse musculaire. C’est généralement une maladie acquise, d’origine immunologique, due à l’altération des récepteurs nicotiniques neuromusculaires par des anticorps. Il existe aussi des formes d’origine génétique, provenant d’un défaut de la synthèse ou de la libération d’acétylcholine ou d’une atteinte des récepteurs neuromusculaires.
Au niveau du système nerveux central
La stimulation des récepteurs nicotiniques du système nerveux central entraîne, par ouverture des canaux cationiques, une dépolarisation dont les conséquences sont encore mal précisées.
Les rôles respectifs des récepteurs muscariniques et nicotiniques dans les effets de l’acétylcholine au niveau du système nerveux central sont difficiles à discerner.
Il y a une déficience cholinergique dans la maladie d’Alzheimer, démence marquée par des troubles de la mémoire, ce qui a conduit à essayer en thérapeutique divers cholinomimétiques directs et indirects.