Les inhibiteurs de la sous-unité ribosomale 30 S ont des propriétés antibiotiques. On y classe les tétracyclines et les aminosides.
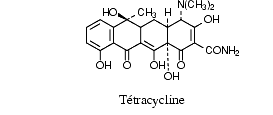
Tétracyclines
Les tétracyclines dites de première génération sont la tétracycline et l’oxytrétacycline, celles de la deuxième génération, la doxycycline et la minocycline.
Les tétracyclines inhibent la synthèse protéique en se fixant à la sous-unité 30 S des ribosomes. Ils s’opposent à la fixation de l’amino-acyl-tRNA sur l’accepteur constitué par le complexe mRNA-ribosome, ce qui arrête la synthèse protéique.
Leur spécificité d’action sur les bactéries provient de différences dans les ribosomes bactériens et surtout de différences de pénétration dans le cytoplasme. Après diffusion passive ou passage à travers des canaux porines de la paroi des germes Gram négatif, les tétracyclines traversent la membrane cytoplasmique par transport actif, faisant peut-être intervenir un transporteur présent chez certaines bactéries seulement.
Les tétracyclines ont une activité antibiotique de type bactériostatique, à large spectre, touchant différentes bactéries Gram positif et Gram négatif ainsi que sur les Rickettsies, Mycoplasmæ, Chlamydiæ, mais une résistance acquise est fréquemment observée.
Elles ont également, en particulier la doxycycline, une activité antipaludique à la fois préventive et curative, de mécanisme mal connu.
Les tétracyclines, et en particulier la doxycycline, inhibent les métalloprotéinases du tissu fondamental appelées MMT (matrix metalloproteinases), enzymes à zinc qui, en hydrolysant certaines protéines, favorisent la dissémination des métastases cancéreuses.
Sur le plan pharmacocinétique, l’absorption digestive des tétracyclines comme la doxycycline et la minocycline est voisine de 100%, elle est meilleure à jeun qu’après un repas. La prise de sels minéraux, aluminium, calcium, magnésium, fer ou bismuth sous diverses formes, réduit l’absorption digestive des tétracyclines en formant avec elles des chélates insolubles.
|
VIBRAMYCINE N* Cp |
|
Les tétracyclines, qui ont une grande affinité pour le tissu osseux, peuvent entraîner en cas d’administration à l’enfant au dessous de huit ans des dyschromies dentaires ou des hypoplasies de l’émail. Elles peuvent également être à l’origine de troubles hématologiques (thrombopénie, neutropénie), de réactions de phototoxicité et de troubles digestifs (apparition de diarrhées, parfois à Clostridium difficile, hépatites).
Les tétracyclines sont contre-indiquées chez la femme enceinte en fin de grossesse, ainsi que chez la femme qui allaite, car il y a risque d’anomalies dentaires chez l’enfant. Le risque d’atteinte hépatique serait plus élevé avec la minocycline qu’avec la doxycycline.
Les tétracyclines sont parfois utilisées d’une manière prolongée, de un à quelques mois, dans le traitement de l’acné. La doxycycline ( Doxypalu*) est utilisée pour la prévention du paludisme chez le voyageur en cas de résistance, de contre-indication ou d’intolérance à la méfloquine (Lariam*).
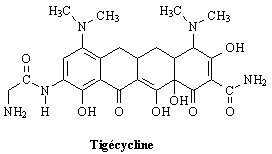
La tigécycline est une nouvelle tétracycline active sur des germes gram positifs et négatifs résistants aux tétracyclines classiques. Elle a été commercialisée aux USA courant 2005 sous le nom de Tygasil*. La tigécycline est administrée par voie intra-veineuse 2 fois par jour.
Aminosides ou aminoglycosides
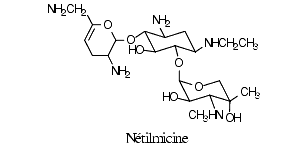
Les premiers aminosides ont été la streptomycine et la néomycine, suivies de la gentamicine, l’amikacine, la nétilmicine, la dibékacine, la tobramycine et plus récemment l’isépamicine.
Les aminosides sont constitués de deux ou plusieurs sucres aminés liés par une fonction glycosidique à un noyau hexose. Leurs fonctions amines sont ionisées formant des polycations.
Les aminosides, antibiotiques bactéricides, diffusent dans les bactéries à travers les canaux porines jusqu’à l’espace périplasmique. Leur pénétration à travers la membrane cytoplasmique est active et nécessite un apport d’énergie et la présence d’oxygène. Lorsque l’aminoside est en permanence présent au contact d’un germe sensible, il y a inhibition de sa pénétration à travers la membrane cytoplasmique. Cette constatation explique l’intérêt de l’administration discontinue des aminosides
Les aminosides perturbent la synthèse protéique bactérienne en se fixant sur les ribosomes de la sous-unité 30 S. Sans doute en raison de leur caractère polycationique, ils déplacent les ions magnésium. L’altération de la membrane bactérienne est la conséquence de la perturbation de la synthèse protéique et de leur effet direct sur elle.
La résistance aux aminosides peut provenir d’un défaut de leur pénétration dans le cytoplasme bactérien, de leur inactivation par biotransformations sous l’influence d’enzymes, phosphorylase, acétylase, synthétisées sous la dépendance de plasmides, d’une modification de la structure des ribosomes empêchant la fixation de l’antibiotique.
Pharmacocinétique
Les aminosides sont ionisés dans les milieux biologiques sous forme de polycations, et ne sont pas absorbés par le tube digestif, leur absorption étant inférieure à 1%.
Leur distribution est essentiellement extracellulaire : de fortes concentrations sont trouvées dans le rein, l’endolymphe et la périlymphe de l’oreille interne, ce qui explique leur toxicité rénale et cochléaire. La concentration atteinte dans le liquide céphalorachidien après administration parentérale est faible, inférieure à 10% de celle que l’on trouve dans le plasma.
Leur élimination urinaire est largement prédominante et ils s’accumulent dans l’organisme en cas d’insuffisance rénale. Dans la mesure où les aminosides ne diffusent pas dans les tissus graisseux, l’adaptation de leur posologie devrait tenir compte seulement du volume de la masse maigre.
Une seule administration par jour d’aminosides au lieu de deux suffirait pour obtenir un bon effet antibiotique tout en réduisant leur toxicité. La détermination systématique des concentrations plasmatiques (pics, vallées) au cours du traitement permet d’éviter les intoxications et les concentrations insuffisantes.
Indications
Les aminosides sont actifs sur les bacilles Gram négatif aérobies, Escherichia coli, Proteus, Kbelsiella pneumoniae, bacille pyocyanique, et sur certains germes Gram positif tels que le staphylocoque, mais ce dernier devient résistant, sauf peut-être à l’amikacine. Ils sont peu ou pas actifs sur les germes anaérobies. L’amikacine a également un effet antituberculeux.
La streptomycine, qui a été le premier antibiotique antituberculeux efficace, est habituellement remplacée par la rifampicine qui inhibe la RNA polymérase bactérienne.
Elle n’est plus guère commercialisée ; en France on la trouve sous le nom de Streptomycine Panpharma*. L’isépamycine n’est commercialisée que dans quelques pays .
| Streptomycine | STREPTOMYCINE* Inj |
Les antibiotiques qui lysent directement la paroi des bactéries comme les ß-lactamines renforcent l’action des aminosides. Par contre, certains antibiotiques qui inhibent eux-mêmes la synthèse protéique, comme le chloramphénicol, réduisent l’efficacité des aminosides
Effets indésirables
Leur toxicité est essentiellement rénale, cochléaire et neuromusculaire.
- Toxicité rénale
- Ototoxicité
- Les aminosides peuvent donner des atteintes cochléaires et vestibulaires par altération des cellules sensorielles, secondaire, peut-être, à la stimulation des récepteurs NMDA par l’antibiotique.
- Les atteintes vestibulaires se traduisent par des vertiges, des vomissements, des céphalées et de l’ataxie, qui disparaissent habituellement à l’arrêt du traitement.
- Les atteintes cochléaires se traduisent par des bourdonnements et une diminution de l’acuité auditive, pouvant aller jusqu’à la surdité définitive. La nétilmicine serait le moins toxique des aminosides pour l’oreille.
- Toxicité neuromusculaire
- Au niveau de la plaque motrice, les aminosides peuvent réduire à la fois la libération d’acétylcholine et la sensibilité des récepteurs nicotiniques. Des apnées ont été déclenchées par l’administration d’aminosides à des malades venant de subir une intervention chirurgicale comportant l’utilisation de curarisants de type d-tubocurarine.
- La néomycine a une activité antibiotique de même type que les autres aminosides mais, en raison de sa toxicité, elle n’est pas utilisée par voie générale. Administrée par voie orale, elle n’est guère absorbée par le tube digestif et a été utilisée dans le traitement des diarrhées infectieuses à germes sensibles (entéro-bactéries, Escherichia coli, Proteus, Kbelsiella, Enterobacter). Elle est également présente dans plusieurs spécialités destinées à traiter des infections cutanéo-muqueuses.
- La spectinomycine est un antibiotique du type aminosides, très actif contre les gonocoques. Elle est utilisée dans le traitement des blennorragies, urétrites chez l’homme et cervicites chez la femme.
- La mupirocine est un antibiotique produit par Pseudomonas fluorescens, actif contre les staphylocoques. Elle inhibe la synthèse protéique en se fixant à l’isoleucyl-tRNA synthétase. Elle est commercialisée sous forme de pommade nasale, utilisée pour éradiquer le portage de Staphylococcus aureus dans les infections récidivantes et éviter leur extension.
- Le fomivirsen est un produit à part: c’est un nucléotide antisens qui neutralise le mRNA du cytomégalovirus et inhibe sa traduction en protéines, ce qui aboutit à une inhibition de la replication. Il est utilisé en injection locale dans le traitement de la rétinite à cytomégalovirus. Il a été commercialisé mais ne l’est plus actuellement.