Ces médicaments ne modifient pas la synthèse des facteurs de la coagulation mais modifient leurs effets, en particulier celui de la thrombine et du facteur Xa, soit directement soit indirectement.
Inhibiteurs directs de la thrombine
La thrombine est la protéase qui provoque la transformation du fibrinogène en fibrine. C’est une enzyme que l’on peut inhiber en agissant, soit au niveau de son site actif, soit en dehors de celui-ci, soit encore en agissant sur elle lorsqu’elle est dans un état intermédiaire dit de transition.
L’effet anticoagulant des antagonistes de la thrombine est mesuré par le test «temps de céphaline activé» ou TCA et leur posologie adaptée en fonction des résultats de ce test.
Les antagonistes de la thrombine sont des polypeptides et des produits de synthèse non peptidiques.
- Antithrombiniques directs peptidiques, analogues de l’hirudine, préparations injectables
- L’hirudine : polypeptide de 65 acides aminés, extrait de la salive de sangsue, Hirudo medicinalis, qui a une très grande affinité pour la thrombine et forme avec elle un complexe équimoléculaire (1/1) inactif. L’hirudine obtenue par génie génétique et appelée recombinante n’est pas commercialisée mais ses analogues, la lépirudine, la désirudine et bivalirudine, le sont.
- La lépirudine : polypeptide de 65 acides aminés, identique à l’hirudine naturelle à l’exception de deux acides aminés mais ayant la même configuration spatiale qu’elle, est obtenue par génie génétique. Elle s’administre par voie intraveineuse en bolus et en perfusion. Elle s’élimine en grande partie par le rein et sa posologie doit être réduite en cas d’insuffisance rénale. Les indications de la lépirudine sont la prévention immédiate et le traitement de la maladie thrombo-embolique, chez les malades qui ont une thrombopénie de type II à l’héparine. Le principal risque du traitement par la lépirudine est l’hémorragie. Par ailleurs la lépirudine étant une protéine, elle peut induire la formation d’anticorps.
- La désirudine, ou disulfatohirudine, diffère de l’hirudine naturelle par l’absence d’un groupe sulfate. Elle est obtenue par génie génétique chez la levure Saccharomyces cerevisiae. Elle s’est montrée plus efficace qu’une héparine de bas poids moléculaire dans la prévention des thromboses veineuses profondes après chirurgie orthopédique et est prescrite dans cette indication. La désirudine est administrée par voie intraveineuse à raison de deux injections par jour. Elle s’élimine essentiellement dans les urines et sa posologie doit être réduite en fonction du degré de l’insuffisance rénale. La commercialisation de la désirudine, Revasc*, a été arrêtée en France en octobre 2010.
- La bivalirudine est un peptide de 20 acides aminés, analogue de l’hirudine ayant, selon son AMM, une indication restreinte : l’obtention d’un effet anticoagulant chez les patients subissant une intervention coronaire percutanée. Dans cette indication, elle donne des résultats globalement similaires à ceux de l’association héparine et abciximab. Chez des malades ayant des antécédents de thrombopénie à l’héparine on peut la préférer. Elle s’administre par voie intraveineuse en bolus.
Commercialisée d’abord aux USA sous le nom d’Angiomax*, elle a été commercialisée en France courant 2005 sous le nom d’Angiox*, réservé à l’usage hospitalier.
Bivalirudine
Angiox* Injectable IV
- L’hirudine : polypeptide de 65 acides aminés, extrait de la salive de sangsue, Hirudo medicinalis, qui a une très grande affinité pour la thrombine et forme avec elle un complexe équimoléculaire (1/1) inactif. L’hirudine obtenue par génie génétique et appelée recombinante n’est pas commercialisée mais ses analogues, la lépirudine, la désirudine et bivalirudine, le sont.
- Antithrombiniques directs non peptidiques, actifs par voie buccale
Des inhibiteurs de la thrombine, actifs par voie buccale, sont en cours de commercialisation ; leurs dénominations communes se terminent par « gatran ». Les premiers produits comme le ximélagatran, prodrogue du mélagatran, ont été abandonnés.Le dabigatran, inhibiteur non peptidique de la thrombine, est absorbé par le tube digestif sous la forme de dabigatran etexilate, prodrogue, qui est hydrolysée dans l’organisme en dabigatran. Le dabigatran a obtenu son AMM en 2008 sous le nom de Pradaxa*, gélules à 75 et 110 mg, pour l’indication prévention des troubles thrombo-emboliques après arthroplastie de la hanche et du genou. Il est actif dans la prévention des troubles thrombo-emboliques de la fibrillation auriculaire.
Dabigatran PRADAXA*, Comprimés à 110 et 75 mg
Inhibiteurs directs du facteur Xa
Plusieurs inhibiteurs directs du facteur Xa sont aussi en cours d’étude ; leur intérêt est de prévenir la formation de thrombine.
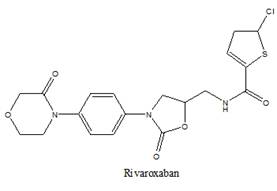
Le rivaroxaban est un inhibiteur sélectif direct du facteur Xa, actif par voie orale. Au cours des essais cliniques, administré par voie orale, il a donné des résultats équivalents à ceux de l’énoxaparine, utilisée en injection sous-cutanée. Le rivaroxaban est commercialisésous le nom de Xarelto* avec comme indication : prévention des troubles thrombo-emboliques après arthroplastie de la hanche et du genou.
| Rivaroxaban | XARELTO, Comprimés à 10 mg |
Remarque : Il n’y a pas aujourd’hui d’antidotes aux antagonistes des inhibiteurs directs de la thrombine et du facteur Xa utilisables en thérapeutique. On peut penser que des aptamères (en anglais aptamer) pourront jouer ce rôle d’antidotes. Les aptamères sont des molécules de DNA et surtout de RNA ayant une très grande affinité pour d’autres molécules, notamment des protéines auxquelles elles se fixent et qu’elles neutralisent. Des travaux concernant aptamères et coagulation ont été publiés mais les applications possibles des aptamères dépassent la coagulation.
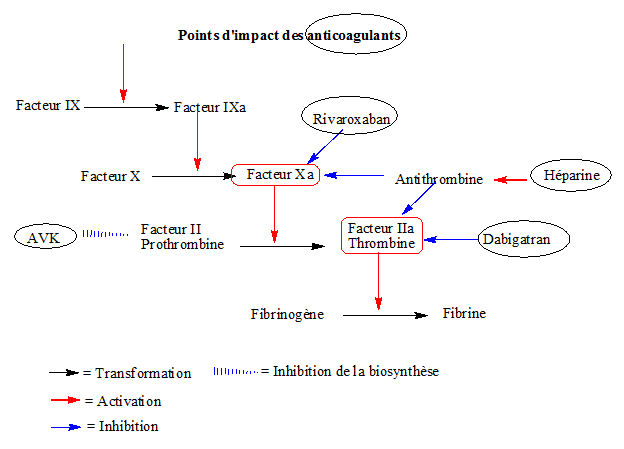
Inhibiteurs indirects de la thrombine et du facteur Xa
L’héparine et les héparines de bas poids moléculaires (HBPM) ainsi que les héparinoïdes comme le danaparoïde inhibent la thrombine et le facteur Xa en activant l’antithrombine III.
Structure chimique
L’héparine est un polysaccharide présent dans divers tissus, notamment le poumon et l’intestin. Sa concentration dans le plasma du sujet sain est très faible et on ne connaît pas son éventuel rôle physiologique.
Les héparines utilisées en thérapeutique sont des mucopolysaccharides anioniques portant des charges négatives, constitués de glucosaminoglycane. Elles sont préparées à partir de tissus d’animaux, surtout le poumon de bœuf et l’intestin de porc. En fonction du degré de fragmentation, leur poids moléculaire varie entre 4 000 et 30 000. L’héparine standard non fractionnée utilisée depuis de très nombreuses années a un poids moléculaire voisin de 30 000. Les HBPM ont un poids moléculaire d’environ 5 000 et sont obtenues par fragmentation de l’héparine.
Ces héparines comportent des séquences pentasaccharidiques communes mais diffèrent par leur longueur et leur action préférentielle sur les facteurs Xa ou IIa.
Le danaparoïde est un mélange de glycosaminoglycanes sulfatés : héparane, dermatane et chondroïtine, obtenus à partir de la muqueuse intestinale de porc. Le danaparoïde se rapproche des HPBM par son poids moléculaire (5 500) mais s’en différencie par sa composition chimique. Il ne contient pas de fragments d’héparine.
Action anticoagulante
Par eux-mêmes, les héparines et le danaparoïde sont inactifs. Ils exercent leur effet anticoagulant en activant des protéines, notamment l’antithrombine et accessoirement le cofacteur II de l’héparine.
L’héparine standard accélère environ 1000 fois la vitesse d’inactivation des protéases par l’antithrombine. Elle forme avec l’antithrombine un complexe binaire qui interagit avec une extrême rapidité avec les facteurs IIa, Xa et accessoirement IXa, XIa et XIIa.
L’héparine standard neutralise d’une manière à peu près identique les facteurs IIa et Xa. Les HBPM neutralisent préférentiellement le facteur Xa.
En cas de déficience constitutionnelle en antithrombine, le risque de thrombose est accru et l’activité de l’héparine est considérablement réduite. Pour traiter les thromboses provoquées par cette déficience, le recours à un inhibiteur direct de la thrombine comme la lépirudine peut être nécessaire.
Le cofacteur II est une glycoprotéine présente dans le sang et formée d’une seule chaîne polypeptidique d’un poids moléculaire de 65 000. Le cofacteur II et l’héparine standard forment un complexe qui inactive seulement la thrombine.
- Héparine standard
- A doses pharmacologiques, elle a une action anticoagulante évidente in vitro (un sang recueilli sur héparine ne coagule pas) et in vivo.
- In vivo, l’efficacité anticoagulante de l’héparine standard dépend de l’état du malade. Une dose suffisante pour entraîner une hypocoagulabilité importante chez un sujet sain, peut ne pas avoir d’efficacité chez un malade ayant une thrombose. Il est donc nécessaire d’adapter la posologie en fonction de l’état du malade.
- La durée d’action de l’héparine standard est relativement courte – sa demi-vie est d’environ une heure – mais augmente avec la dose.
- Le contrôle de l’activité anticoagulante de l’héparine standard s’effectue à l’aide du test dit temps de céphaline activée ou TCA qui doit être égal à deux fois celui du témoin.
- In vivo, l’efficacité anticoagulante de l’héparine standard dépend de l’état du malade. Une dose suffisante pour entraîner une hypocoagulabilité importante chez un sujet sain, peut ne pas avoir d’efficacité chez un malade ayant une thrombose. Il est donc nécessaire d’adapter la posologie en fonction de l’état du malade.
- A doses pharmacologiques, elle a une action anticoagulante évidente in vitro (un sang recueilli sur héparine ne coagule pas) et in vivo.
- Héparines de bas poids moléculaires (HBPM)
- Il s’agit de la daltéparine, la nadroparine, l’énoxaparine et la tinzaparine. La reviparine, Clivarine*, n’est plus disponible en France.
En dehors de leur poids moléculaire plus faible que celui de l’héparine standard, les HBPM ont une activité anti-Xa supérieure à celle de l’héparine et une activité anti-IIa plus faible.- Si on donne un coefficient 1 au rapport Xa sur IIa pour l’héparine, ce rapport est de l’ordre de 10 pour les HBPM. L’activité anticoagulante des HBPM in vitro est plus faible que celle de l’héparine standard, en relation avec un moindre effet anti-IIa.
- La demi-vie des HBPM est de 5 à 6 heures, ce qui permet de réduire la fréquence de leur administration.
- L’activité anticoagulante des HBPM est moins dépendante de l’importance de l’état thrombotique du malade que celle de l’héparine. La posologie des HBPM est plus facile à établir que celle de l’héparine standard. Le contrôle de leur activité anticoagulante qui s’effectue par le dosage de l’activité anti-Xa, n’est pas nécessaire en pratique courante.
- Les HBPM provoquent moins d’hémorragies et de thrombopénies graves que l’héparine standard. Pour le moment les HBPM sont plus coûteuses que l’héparine standard mais l’adaptation de leur posologie est plus simple et nécessite moins de contrôles biologiques, ce qui réduit partiellement la différence de prix de revient du traitement.
- Si on donne un coefficient 1 au rapport Xa sur IIa pour l’héparine, ce rapport est de l’ordre de 10 pour les HBPM. L’activité anticoagulante des HBPM in vitro est plus faible que celle de l’héparine standard, en relation avec un moindre effet anti-IIa.
- Il s’agit de la daltéparine, la nadroparine, l’énoxaparine et la tinzaparine. La reviparine, Clivarine*, n’est plus disponible en France.
- Héparinoïdes : danaparoïde et fondaparinux
- Le danaparoïde est un mélange de glycosaminoglycanes extraits de la muqueuse intestinale de porc. Il ne contient pas de fragments d’héparine et n’est donc pas chimiquement une héparine de bas poids moléculaire.
- La durée d’inhibition de l’activité Xa après une administration de danaparoïde est de 25 heures, durée aussi appelée demi-vie. Comme les HPBM, il inhibe préférentiellement le Xa et non le IIa.
- L’un des intérêts du danaparoïde est de donner un faible pourcentage de réactions croisées avec l’héparine standard et les HPBM au niveau plaquettaire. En cas de thrombocytopénie induite par eux, il peut donc leur être substitué après vérification de l’absence de réactions croisées par un test d’agrégation plaquettaire.
- La durée d’inhibition de l’activité Xa après une administration de danaparoïde est de 25 heures, durée aussi appelée demi-vie. Comme les HPBM, il inhibe préférentiellement le Xa et non le IIa.
- Le danaparoïde est un mélange de glycosaminoglycanes extraits de la muqueuse intestinale de porc. Il ne contient pas de fragments d’héparine et n’est donc pas chimiquement une héparine de bas poids moléculaire.
- Le fondaparinux est un pentasaccharide de synthèse qui inhibe sélectivement le facteur Xa en activant l’antithrombine III. L’indication retenue pour le fondaparinux est la prévention des troubles thrombo-emboliques veineux après les grosses interventions chirurgicales orthopédiques sur le membre inférieur, hanche et genou.
Caractéristiques pharmacocinétiques
Les héparines sont peu absorbées par le tube digestif et s’administrent par voie parentérale, intraveineuse ou sous-cutanée, selon les produits.
L’héparine s’accumule dans l’endothélium vasculaire où sa concentration peut être 100 fois plus élevée que dans le plasma. Par la suite, l’endothélium la libère progressivement.
Sur le plan pharmacocinétique, le point essentiel est que l’héparine standard ne traverse pas le placenta et peut être utilisée chez la femme enceinte. Les HBPM et les héparinoïdes pourraient traverser le placenta et, en pratique, leur utilisation chez la femme enceinte est déconseillée.
En matière de coagulation, il y a souvent ambiguïté entre les données pharmacocinétiques, c’est-à-dire la mesure de la concentration plasmatique du médicament administré et celle de ses effets. Le plus souvent ce sont les effets sur la coagulation que l’on mesure et non la concentration.
Indications
L’héparine et les HBPM sont utilisées pour prévenir et traiter les accidents thrombo-emboliques veineux et artériels. Elles s’administrent habituellement par voie parentérale, intraveineuse ou sous-cutanée. Chaque spécialité existe sous plusieurs présentations: les plus faiblement dosées sont destinées au traitement préventif et les plus fortes au traitement curatif.
Les HBPM tendent à remplacer l’héparine standard dans ses indications préventives et curatives car elles entraînent moins d’effets indésirables graves mais c’est l’héparine standard qui est associée aux antagonistes du récepteur de la glycoprotéine IIb/IIIa.
L’héparine et les HBPM d’action immédiate constituent le traitement anticoagulant initial, pendant une durée généralement de moins de 10 jours, et sont si nécessaire remplacées ensuite par les AVK. Cependant dans certaines indications, par exemple après chirurgie de la hanche la durée du traitement par HBPM peut être prolongée plus d’un mois.
Effets indésirables
Le risque de saignement et d’hémorragie est une conséquence de tout traitement anticoagulant.
Le principal danger des héparines est la thrombopénie. On en distingue deux types :
- les thrombopénies précoces, dites de type I, modérées, apparaissant du 2e au 5e jour, voire un peu plus tard, qui sont des formes bénignes avec une chute des plaquettes autour de 100 000/mm3.
- les thrombopénies plus tardives, dites de type II, d’origine immunologique, qui surviennent après le 8e jour. Ce sont des formes graves pouvant s’accompagner de thromboses plaquettaires avec des accidents ischémiques parfois mortels. Elles nécessitent le contrôle de la numération plaquettaire tous les deux jours pendant les deux première semaines de traitement. Ce type de thrombopénie s’explique ainsi : l’héparine, et à un moindre degré les HBPM, peuvent former avec le facteur-4-plaquettaire un complexe, lequel suscite la formation d’anticorps et l’interaction complexe-anticorps active les plaquettes provoquant l’agrégation plaquettaire et des thromboses. Le danaparoïde serait moins susceptible de donner cette interaction.
- Le risque de thrombopénie grave est beaucoup moindre avec des HBPM lorsqu’elles sont utilisées d’emblée et non en remplacement de l’héparine standard si celle-ci a déjà induit une thrombopénie grave. Ce risque serait encore beaucoup moindre avec le danaparoïde. Actuellement, en cas de survenue d’une thrombopénie grave provoquée par une héparine il faut la remplacer par le danaparoïde ou, de préférence, la lépirudine.
Les héparines sont, assez rarement, à l’origine de réactions allergiques : urticaire, fièvre, choc exceptionnellement. Mais en 2008, surtout aux USA, plusieurs manifestations allergiques avec chutes de tension, dont certaines mortelles, ont été observées après administration d’héparine sodique. Ces accidents ont été attribués à la présence anormale de chondroïtine persulfatée dans certains lots d’héparine. Des mesures ont été prises pour retirer du commerce les héparines « contaminées ».
Elles peuvent donner également des réactions cutanées (alopécie transitoire) ou des réactions lipodystrophiques après injections sous-cutanées répétées au cours du traitement de longue durée.
Elles peuvent faire apparaître des troubles osseux : l’administration prolongée d’héparine peut donner de l’ostéoporose avec possibilité de fractures spontanées, dont le mécanisme est discuté. Ce risque serait moindre avec les HPBM. Des calcifications métastatiques chez les hémodialysés traités par l’héparine peuvent également se voir.
Antagoniste de l’héparine
La protamine est un polypeptide polycationique (charges +) comportant environ 67% d’arginine. Elle forme avec l’héparine, mucopolysaccharide polyanionique, un précipité. La protamine neutralise l’action anticoagulante de l’héparine, mais elle neutralise plus efficacement les effets de l’héparine standard que ceux des HBPM.
La protamine existe sous forme de solution injectable, à administrer lentement par voie intraveineuse, en principe 1 ml neutralise 1000 unités d’héparine.
Elle est aussi utilisée dans les préparations d’insuline à effet prolongé car elle forme avec l’insuline un complexe qui, après injection, libère progressivement l’insuline.
Des expérimentations chez l’animal ont montré que la protamine pouvait réduire le développement de certaines tumeurs en inhibant l’angiogenèse.
| PROTAMINE* Inj |
